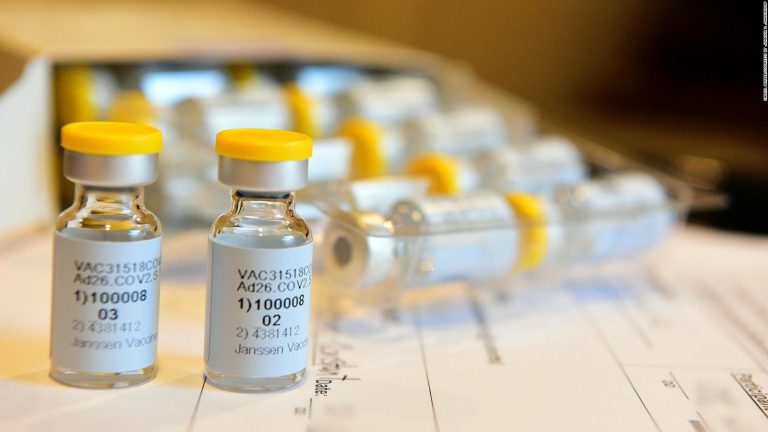
Johnson & Johnson anunció su ensayo clínico Fase 3, a gran escala y en varios países para su vacuna candidata contra el COVID-19, JNJ-78436735, que está siendo desarrollado por Janssen Pharmaceutical Companies.
El inicio del ensayo clínico ENSEMBLE comienza tras los resultados provisionales positivos del estudio clínico Fase 1/2a de la compañía, que demostró que el perfil de seguridad y la inmunogenicidad después de una dosis única de la vacuna respaldan el avance en el desarrollo.
Estos resultados se han sometido a medRxiv y se publicarán en línea posteriormente. Con base en estos resultados y en discusiones con la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA), ENSEMBLE reclutará hasta 60 mil voluntarios en tres continentes y estudiará la seguridad y eficacia de una dosis única de la vacuna versus placebo en la prevención de COVID-19.
Johnson & Johnson ha continuado ampliando su capacidad de manufactura y sigue encaminada a cumplir con su objetivo de proporcionar hasta mil millones de dosis de la vacuna cada año. La Compañía está comprometida con poner a disposición del público una vacuna asequible sin fines de lucro para su uso de emergencia en la pandemia y prevé que los primeros lotes de la vacuna COVID-19 estarán disponibles para su autorización de uso de emergencia a principios de 2021, si demuestra que es segura y eficaz.
La compañía desarrollará y probará su vacuna candidata COVID-19 con altos estándares éticos y principios científicos rigurosos. La Compañía está comprometida con la transparencia y el intercambio de información relacionada con el estudio clínico Fase 3 ENSEMBLE – incluyendo el protocolo del estudio.
«A medida que el COVID-19 continúa impactando la vida diaria de las personas en todo el mundo, nuestro objetivo sigue siendo el mismo: aprovechar el alcance global y la innovación científica de nuestra compañía para ayudar a poner fin a esta pandemia«, dijo Alex Gorsky, Chairman and Chief Executive Officer, Johnson & Johnson.
“Como la compañía del cuidado de la salud más grande a nivel mundial, estamos aportando nuestras mejores mentes científicas y rigurosos estándares de seguridad, en colaboración con los reguladores, para acelerar la lucha contra esta pandemia. Este hito fundamental demuestra nuestros esfuerzos centrados en una vacuna contra el COVID-19 que se basan en la colaboración y el compromiso profundo con mantener procesos científicos rigurosos. Estamos comprometidos con la transparencia de los ensayos clínicos y con el intercambio de información relacionada con nuestro estudio, incluyendo los detalles del protocolo del estudio”.
“Seguimos enfocados en desarrollar con sentido de urgencia una vacuna contra el COVID-19, que sea segura y eficaz para las personas de todo el mundo”, dijo Paul Stoffels, M.D., Vice Chairman of the Executive Committee and Chief Scientific Officer, Johnson & Johnson. «Valoramos enormemente el apoyo y la colaboración de nuestros socios científicos y las autoridades sanitarias mundiales, mientras nuestro equipo de expertos global trabaja incansablemente en el desarrollo de la vacuna y en la ampliación de nuestra capacidad de producción con el objetivo de entregar una vacuna para autorización de uso de emergencia a principios de 2021».
La vacuna candidata COVID-19 de Janssen aprovecha la plataforma de tecnología AdVac® de la compañía, que también se utilizó para desarrollar y fabricar la vacuna contra el Ébola de Janssen, aprobada por la Comisión Europea, y construir sus vacunas candidatas contra el Zika, el VSR y el VIH. La plataforma tecnológica AdVac® a la fecha se ha utilizado para vacunar a más de 100 mil personas en todos los programas de investigación de vacunas de Janssen.
Gracias a la tecnología AdVac® de Janssen, se estima que, si tiene éxito, la vacuna en el momento de su lanzamiento sea estable durante 2 años a -20°C y al menos tres meses a 2-8° C. Esto hace que sea compatible con los canales de distribución estándar de vacunas y que no requiera de una nueva infraestructura para hacerla llegar a las personas que la necesitan.